
调节T细胞,天使还是魔鬼?
发布时间:2017-09-02 22:55所属分类:国际快讯浏览:次
调节T细胞(Treg细胞),是一类调控机体免疫功能的细胞群,能维持免疫系统对自身成分的耐受,使机体保持免疫稳态。这类细胞以表达Foxp3、CD25、CD4为细胞表型特征。在过去20年内,研究已经证实了Treg细胞在感染、肿瘤、器官移植、同种异体
调节T细胞(Treg细胞),是一类调控机体免疫功能的细胞群,能维持免疫系统对自身成分的耐受,使机体保持免疫稳态。这类细胞以表达Foxp3、CD25、CD4为细胞表型特征。在过去20年内,研究已经证实了Treg细胞在感染、肿瘤、器官移植、同种异体胎儿免疫相关疾病方面具有抑制各种途径的病理生理免疫应答的作用。总体上认为,炎症是许多疾病包括糖尿病发生的重要基础,这种Treg细胞抑制炎症反应的作用被认为是对抗炎症,抑制炎症相关疾病发生发展的内在正面力量。不过生物系统几乎没有绝对,任何细胞和分子,在不同的条件下,可能是朋友,也可能是敌人。最近《自然》报道一种新型糖尿病类型,年龄相关糖尿病的4型糖尿病发生过程中,脂肪组织中被认为是天使的Treg细胞,竟然变成促进糖尿病发生的魔鬼。这一细胞的罪恶一面的发现真是让人惊叹。也可以说,这种细胞只是在发挥应该发挥的生物学作用,无所谓天使和魔鬼,我们只不过是从人和功利角度看这个细胞的作用而已。
糖尿病一般是肥胖和不良饮食习惯所导致,但糖尿病也是一种衰老相关疾病,随着年龄增长,糖尿病发生率明显增加。
新研究发现,瘦鼠老年胰岛素抵抗与由体重增加所导致的糖尿病有着不同的细胞基础。研究提出一种新型糖尿病(4型),并指出可能治疗方法。这项研究发布在2015年11月18日的《自然》杂志上,Salk研究所基因表达实验室主任Ronald Evans及Nomis免疫生物学与微生物发病机制基础实验室助理教授郑野是这项研究的共同通讯作者。Evans说:“许多老年人未发展成为糖尿病,是因为没有2型糖尿病的典型风险因子,如肥胖等。我们希望我们的研究发现不仅可促成一些治疗方法,还可以让更多人认识到4型糖尿病是一种独立的糖尿病类型。”
健康人体内胰腺会在饭后分泌胰岛素,向肝脏和肌肉等细胞发出信号,促进这些细胞从血液中摄取葡萄糖。糖尿病患者体内这一机制遭到破坏。有的是胰腺不响应进食分泌胰岛素,有的是胰岛素调节细胞如肌肉和肝细胞对胰岛素反应不敏感,就是发生了胰岛素抵抗。这些情况下餐后血液高水平葡萄糖持续更长时间,高血糖对血管会带来伤害,导致肢体残疾甚至心脑等重要器官功能障碍,甚至是死亡等健康危害。
糖尿病分为1型和2型两类。1型糖尿病是胰腺生成胰岛素的功能障碍,多见于儿童和青少年。2型糖尿病是机体细胞响应胰岛素的功能不足,往往是由肥胖和运动缺乏引起。两种糖尿病的共同表现是血糖高水平。第4类糖尿病多发生在身体消瘦的个体,往往造成一些与阿尔茨海默病相似的症状。Evans想知道为什么一些人在生命晚期体重未增长的情况下也会形成这一疾病。
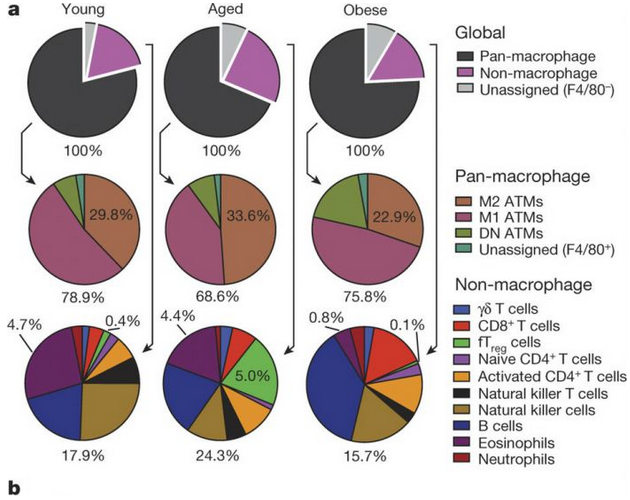
Evans、郑野及同事们着手比较了健康小鼠、肥胖相关糖尿病的小鼠和年龄相关糖尿病小鼠的免疫系统。他们发现,年龄相关糖尿病小鼠脂肪组织内发现高水平调节性T细胞(Tregs)。肥胖相关糖尿病的小鼠尽管有着更多的脂肪组织,但组织中Tregs水平正常。
期刊的第一作者Sagar Bapat说:“我们对这些小鼠脂肪组织中的免疫细胞进行了观察。通过细胞类型计数,很快看到了老年糖尿病小鼠体内的Tregs要多于其他类型动物。”Bapat说,通常Tregs的功能抑制炎症反应。脂肪组织储存和分解能量物质过程中,需要低水平炎症反应协助,新研究表明随着年龄增长,Tregs在脂肪内逐渐累积。当这些细胞数量随着年龄增加到临界点,会完全阻断脂肪组织炎症反应,这会导致脂肪分解过程被中断,造成脂肪沉积,也会在内脏如肝脏等部位累积,这会导致胰岛素抵抗的发生。
郑野说:“通常人们认为,Tregs抑制炎症反应,对身体有益,这一发现与这一传统观点相反,令人意外。”
用一种分子靶向阻断Tregs细胞阻止在脂肪中累积,小鼠不再在老年形成4型糖尿病。但如果小鼠肥胖,阻断脂肪中Tregs细胞不能阻止2型胰岛素抵抗。
Evans说:“结果表明,对于这种类型的糖尿病,减肥治疗并没有意义。治疗方法实际上是去除这些细胞,研究证实有可能实现这一目的。”
研究人员希望阐明Tregs与脂肪组织的确切互作机制,以及正常衰老过程中这些免疫细胞是否在其他器官中累积。他们还计划开展一些研究看这些现象是否也发生于人类。Salk研究所资深研究员Michael Downes说:“我们正与临床医生合作采集来自老年消瘦糖尿病患者的样本,看看这一细胞类型是否也与人类疾病有关。”
上一篇:美国科学家制造出不同头颅的“鬼虫”
下一篇:医生对可穿戴装置的兴趣 担心多于追捧


 李编辑
李编辑

